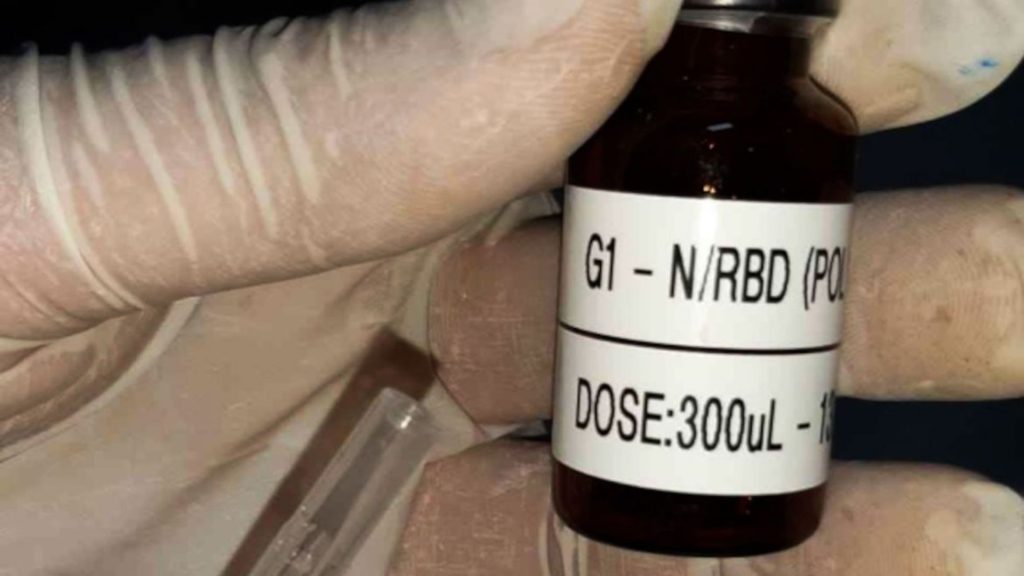
Nesta segunda-feira (3), a Agência Nacional de Vigilância Sanitária (Anvisa) publicou a autorização para a condução de um ensaio clínico que terá como produto investigacional a SpiN-Tec, uma candidata à vacina para Covid-19.
– Envie esta notícia no seu Whatsapp
– Envie esta notícia no seu Telegram
A SpiN-Tec é uma proteína quimérica recombinante que utiliza a proteína SpiN, desenvolvida pelo Centro de pesquisa e produção de vacinas da Universidade Federal de Minas Gerais (CT Vacinas da UFMG).

A autorização aconteceu após a agência analisar os dados das etapas anteriores de desenvolvimento dos produtos, incluindo estudos não clínicos in vitro e em animais, bem como dados preliminares de estudos clínicos em andamento.
RELACIONADAS
+ Brasil registra 8,8 mil casos de Covid-19 e 57 mortes provocadas pela doença, em 24h
+ Pesquisa mostra eficácia da vitamina B12 para atenuar covid-19
+ Anvisa recebe pedido de uso emergencial de nova vacina contra covid da Pfizer
Os resultados obtidos, até o momento, demonstraram um perfil de segurança aceitável da vacina candidata.
De acordo com a Anvisa, trata-se de ensaios clínico em que o produto investigacional será utilizado pela primeira vez em humanos.
O ensaio terá duas partes: “Um ensaio clínico, de fase 1, de dose escalonada para verificar segurança e reatogenicidade do produto investigacional; e outro ensaio clínico, de fase 2, para estudo de segurança e imunogenicidade da SpiN-Tec”.
“O ensaio clínico incluirá participantes saudáveis de ambos os sexos, com idade entre 18 e 85 anos, que completaram o esquema vacinal primário com a Coronavac ou Covishield (Astrazeneca/Oxford), e que receberam uma ou duas doses de reforço com a Covishield ou Comirnaty (Pfizer) há pelo menos seis meses”, informou a Anvisa.
O estudo será financiado pela UFMG, pelo Ministério da Ciência e Tecnologia e Inovação (MCTI), pela Fundação Oswaldo Cruz (Fiocruz) e prefeitura de Belo Horizonte.